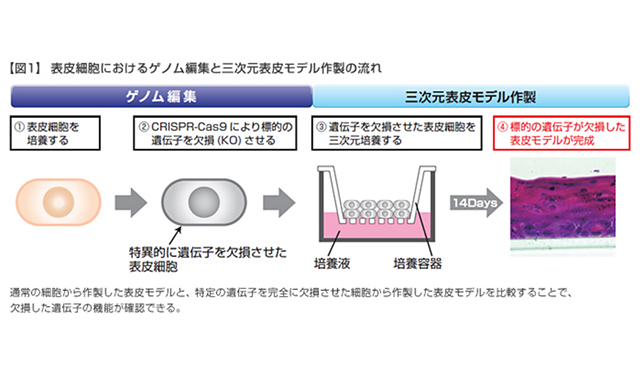
富士フイルムは2017年3月23日、東京医科歯科大学の難波大輔准教授との共同研究で、ゲノム編集技術「CRISPR-Cas9(クリスパー キャスナイン)」を用いてヒト表皮細胞のゲノムを編集し、その細胞を三次元培養した表皮モデルの作製に成功したと発表した。この技術を活用し特定の遺伝子を欠損させることで、加齢による皮膚状態の変化を三次元表皮モデルで再現できるという。
培養した細胞で遺伝子の機能を調べる場合、標的となる遺伝子の発現を弱めた細胞を作製し、通常の細胞と比較するのが一般的だ。その際、標的となる遺伝子の発現を弱めるのにRNA干渉法や薬剤が使われるが、遺伝子の発現は完全には止められない。また、薬剤は標的以外の遺伝子にも影響を及ぼす。
富士フイルムと難波大輔准教授は上述の課題解決に向け、先端のゲノム編集技術「CRISPR-Cas9」を活用し、標的の遺伝子を完全に欠損(KO)させたヒト表皮細胞を用いて表皮モデルを作製する技術開発に取り組んだ。今回の研究では、標的の遺伝子をインスリン様成長因子「IGF-1」の受容体「IGF-1R」とした。IGF-1Rは、IGF-1を受け取って表皮細胞に増殖シグナルを送る役割を担う。この機能を停止させる遺伝子編集を施し、表皮形成時に増殖シグナルがもたらす影響を確認した。
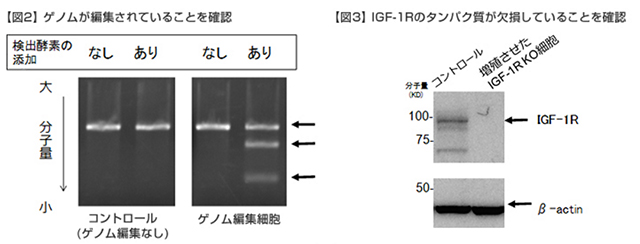
IGF-1Rを狙って編集できるように調整したCRISPR-Cas9を使って、培養したヒト表皮細胞のゲノムを編集し、ゲノム編集の有無を電気泳動法で検証したところ、目的通りにゲノムが編集できていることを確認。その後、ゲノム編集した細胞を増殖させ、ウェスタンブロット法でIGF-1Rタンパク質の有無を調べたところ、増殖した細胞において同タンパク質が完全に欠損していることを確認した。
次いで、IGF-1R KO細胞と通常の表皮細胞の三次元表皮モデルを作製し、培養開始から14日後にそれぞれの切片を観察した。結果、IGF-1R KO細胞を用いた表皮モデルは、通常の表皮細胞の表皮モデルに比べ表皮厚が約半分になり、細胞の分化も低下すると分かった。その理由としては、細胞増殖を促すシグナルがIGF-1Rの欠損により細胞内に伝達されなくなったことが考えられる。以上のことから、IGF-1Rが発する増殖シグナルが表皮層の形成に重要な役割を果たすことが確認できた。
CRISPR-Cas9により作製した、特定の遺伝子を欠損させた表皮細胞は、細胞分裂後も永久に変異が引き継がれるため、欠損した状態を安定的に維持した長期培養が可能となる。また、本技術により遺伝子を欠損させて、意図的に疾患を持った皮膚モデルを作製することも可能になる。富士フイルムは研究成果を積極的に機能性化粧品の開発に応用していくとしている。