- 2022-12-28
- ニュース, 化学・素材系, 技術ニュース
- C1-Cx説, endo-exo説, oxidative boost, Phanerochaete chrysosporium, SDGs, スーパーコンピュータ, セルラーゼ, セルロース, バイオマス, バイオマスプラスチック, バイオ燃料, ミシガン州立大学, 再生可能エネルギー, 分子動力学シミュレーション, 分解酵素, 名古屋大学, 東京大学, 研究, 米国エネルギー省, 静岡大学, 高速原子間力顕微鏡
東京大学は2022年12月24日、同大学大学院農学生命科学研究科や名古屋大学、静岡大学、ミシガン州立大学、米国エネルギー省再生可能エネルギー研究室からなる共同研究チームが、セルロースの表面を溶かして分解する酵素の機能を解明したと発表した。
セルロースは地球上で最も豊富に存在するバイオマスであり、効率良く分解することができれば、得られたグルコースからバイオ燃料やバイオマスプラスチックといったさまざまな化合物を作製することが可能となる。
セルロースは加水分解が難しいものの、自然界にはセルロース分解酵素(セルラーゼ)を用いてセルロースを分解し、消化して栄養源としているきのこやカビ、バクテリアなどの生物が存在する。一方で、そのような酵素によるセルロースの分解メカニズムは未だ解明されていなかった。
東京大学大学院農学生命科学研究科の研究チームは、セルロースの中でも特に分解性が低い結晶性セルロースの酵素による分解を長期にわたり研究している。
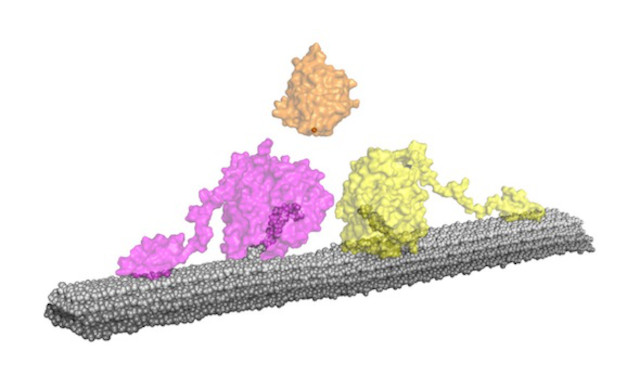
きのこの一種である「Phanerochaete chrysosporium」が生成する溶解性多糖モノオキシゲナーゼ(LPMO)のAA9Dが、その他のCel6A、Cel7Dといったセルロース分解酵素による結晶性セルロースの分解にどのような影響を与えるのかに関する実験を進めていた過程で、AA9Dが自身の生成物である酸化されたオリゴ糖をほとんど出さずに、他の酵素の活性を高めることを発見した。
そこで、名古屋大学の研究チームとの共同研究で、高速原子間力顕微鏡を用いてセルロース表面で働くCel7D分子を観察したところ、AA9Dが一緒に働いている時にセルロース表面を動く酵素分子の数が増加することが判明した。
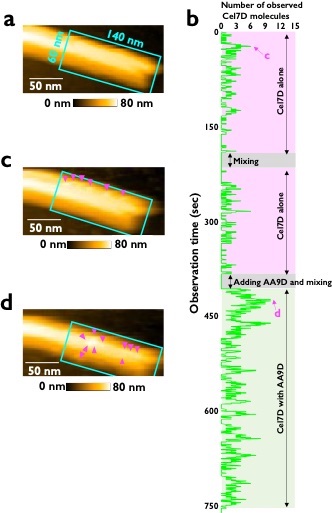
高速原子間力顕微鏡によるセルラーゼ分子の観察
a:酵素を入れる前の結晶性セルロース、b:酵素分子の時間変化、c:Cel7Dのみが反応している時のセルロース表面の様子、d:Cel7DとAA9Dが一緒に反応している様子
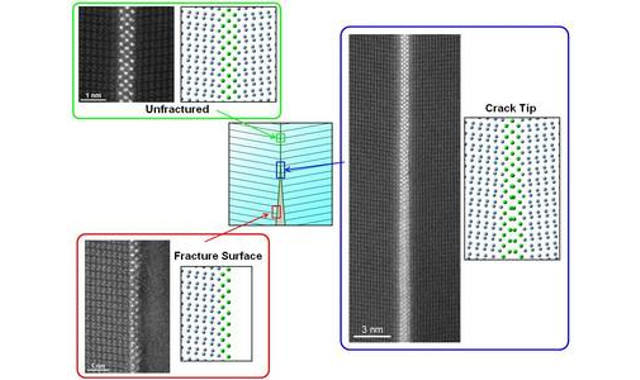
さらに、米国エネルギー省再生可能エネルギー研究室の研究チームとの共同研究により、AA9Dによって酸化されたセルロース表面がどのように変化するのかをスーパーコンピュータを用いて分子動力学シミュレーションした。
AA9Dによって酸化されたセルロースの表面において、酸化されたセルロース分子が浮いてくるのみならず、周りのセルロース分子との水素結合が切断され、そこに水分子が流入して溶解する(非晶化する)ことも判明した。
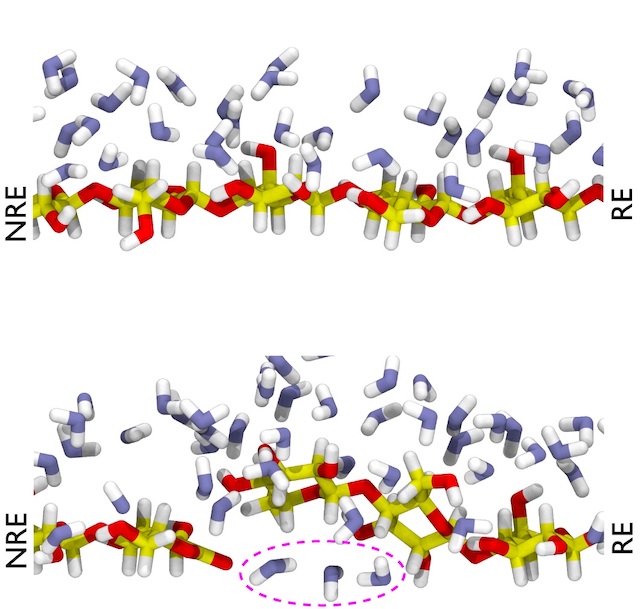
AA9Dによって切断された末端がラクトンになっている部位周辺における水分子の分子動力学シミュレーション結果
上段:結晶性セルロースの表面(コントロール)
下段:AA9Dによって切断された後の結晶表面。点線で囲われているのはセルロース分子の下に流れ込んだ水分子
以上により、LPMOが一度セルロースを酸化的に開裂すると、その周辺の水素結合ネットワークが乱れ、酸化されていないセルロースも水和して非晶化し、結果として他のセルロース分解酵素も非晶化されたセルロース分子を容易に分解可能となり、それらの酵素が反応するとさらにその周辺のセルロースが水和して非晶化されるという連鎖的な反応により、「oxidative boost(酸化的加速。酸化反応がセルロース分解を速めるとする学説)」が起こっていると推察された。
非晶化したセルロースを分子の途中から切断する機構は、1972年に提唱された「endo-exo説」での仕組みと同一だった。また、水和から連鎖するセルロース分解は、Reeseらが1950年に提唱した「C1-Cx説」と同じ仕組みとなっている。
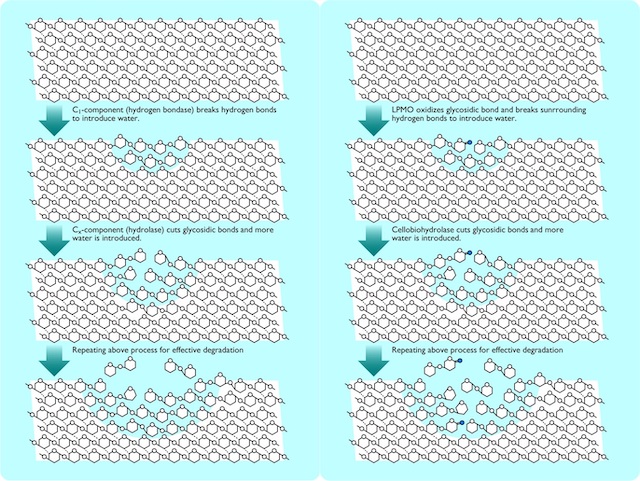
C1-Cx説(左)およびLPMOによるoxidative boost(右)におけるセルロース分子の分解
これらにより、既存のC1-Cx説、endo-exo説、oxidative boostの3つの学説は、同じ現象を異なる視点から見たものであることが明らかになった。
今回の研究結果は、木や草などの主成分であるセルロースの酵素分解に直接応用できる。稲わらやサトウキビバガス(サトウキビの絞りかす)などの未利用のバイオマスや、古紙や建築廃材といったセルロース系のバイオマスを用いて、バイオ化成品やバイオ燃料、バイオプラスチックなどを高効率で生産するにあたっての重要な知見となる。